Les résultats présentés dans ce chapitre regroupent les informations transmises pour les fœtus pour lesquels un examen de génétique moléculaire à visée diagnostique, sur prélèvements invasif et non invasif, a été réalisé.
Les différentes maladies pour lesquelles un diagnostic prénatal est fait par la génétique moléculaire sur prélèvement invasif (tableaux DPN18, DPN19 et DPN20) et non invasif (tableau DPN 24) sont identifiées selon la classification de l’encyclopédie Orphanet. Ainsi, peuvent être comptabilisées comme deux pathologies distinctes deux formes d’une même maladie enregistrées sous deux numéros ORPHA différents. Le numéro ORPHA est un identifiant unique et stable dans le temps, associé à chaque entité de la classification Orphanet des maladies rares. Cette stratégie permet un recueil des données comparables d’une année à l’autre.
La dernière décennie a été marquée par des évolutions technologiques majeures en biologie moléculaire. Alors que les examens étaient initialement ciblés sur un gène, le développement du séquençage massif parallèle a permis d’envisager l’examen simultané de plusieurs gènes. L’étude d’un nombre limité de gènes, le plus souvent dédié à une pathologie ou un groupe de pathologies correspond à une étude dite de « panel de gènes ». L’étude élargie à l’ensemble des exons des gènes (partie codante des gènes) connus correspond à l’« étude de l’exome ». Ces technologies par séquençage haut débit ou NGS sont progressivement devenues accessibles en diagnostic prénatal.
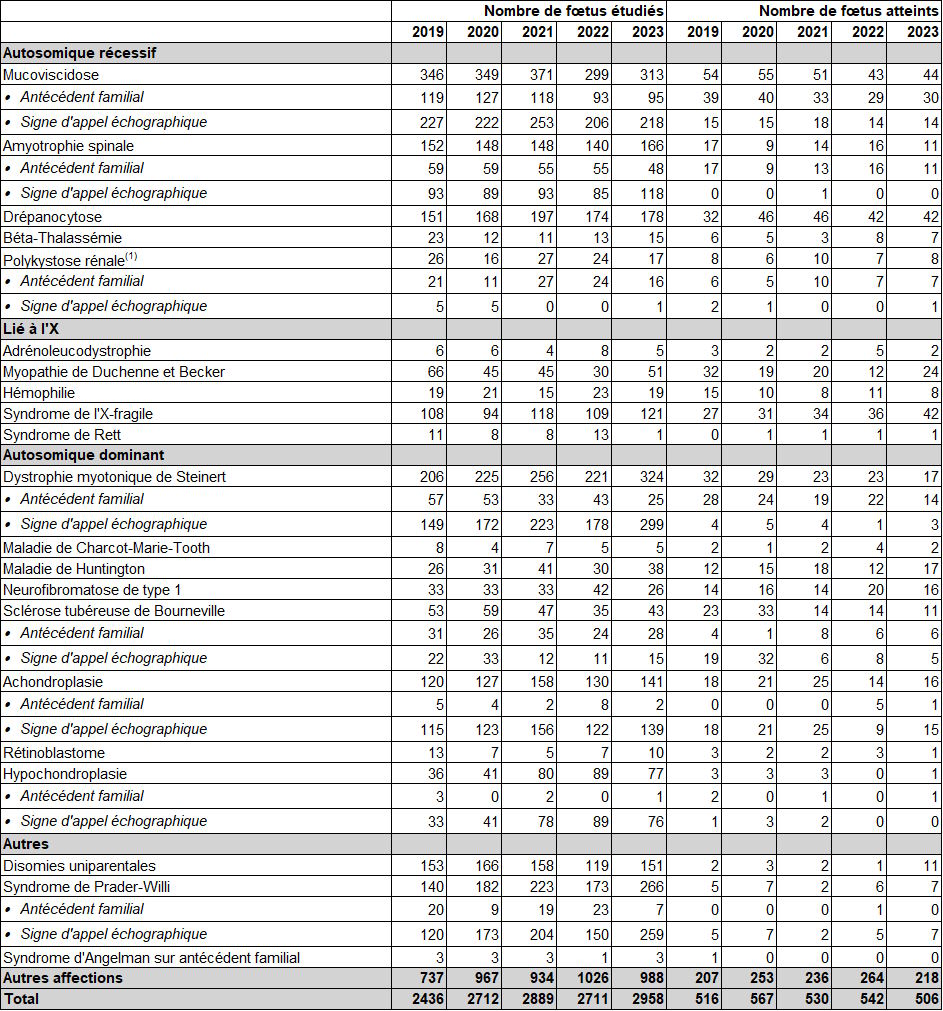
L’activité de diagnostic prénatal en génétique moléculaire ciblée sur une pathologie sur prélèvement invasif a concerné 2 875 fœtus pour plus de 450 maladies génétiques différentes (selon la classification ORPHANET). Ces maladies sont pour la plupart extrêmement rares (tableau DPN19). Toutefois, les 21 maladies décrites dans le tableau DPN18 représentent à elles seules plus des 2/3 (68,6 %) des fœtus étudiés. De très nombreuses maladies génétiques sont si rares qu’elles ne sont l’objet que de quelques prélèvements à visée diagnostique voire d’un unique prélèvement par an, et pour la grande majorité, dans un contexte d’antécédent familial.
En raison de la fréquence dans la population générale, la mucoviscidose reste la maladie la plus fréquemment étudiée, avec un total de 313 fœtus étudiés - soit 218 sur signes d’appels échographiques et 95 sur antécédent familial-, et diagnostiquée avec 44 fœtus atteints. Du fait de leur fréquence dans la population générale et en DPN dans le cadre d’antécédents familiaux, les pathologies comme la drépanocytose, le syndrome de l’X-fragile, la maladie de Duchenne et Becker, maladie de Huntington, sclérose tubéreuse de Bourneville et neurofibromatose de type 1 représentent également une part importante de ces indications et atteintes fœtales avec respectivement : 178, 121, 51, 38, 28, 26 fœtus étudiés, soit un total de 442 fœtus étudiés pour ces 6 pathologies, et de 42, 42, 24, 17, 6, 16 fœtus atteints soit un total de 147 fœtus atteints.
En DPN, l’indication de l’examen de génétique moléculaire peut être posée sur signe d’appel échographique. La présence de signes d’appel quasi-pathognomoniques de certaines maladies génétiques homogènes bien documentées sur le plan moléculaire a comme conséquence un rendement diagnostique de l’examen ciblé élevé. Ainsi, entre 2019 et 2023, 237 examens ont été réalisés dans l’indication d’une sclérose tubéreuse de Bourneville, dont 93 examens pour signe d’appel échographique, parmi lesquels 70 fœtus étaient atteints. Dans l’indication achondroplasie, sur la période de 2019 à 2023, 676 examens ont été réalisés, dont 655 pour signes d’appel échographique parmi lesquels 88 étaient atteints (tableau DPN18).
Lorsqu’un signe échographique peu spécifique est présent, le choix de recourir à un examen ciblé prend en compte le contexte de la grossesse et la fréquence de la survenue de la pathologie ainsi que et la fréquence d’hétérozygotie dans la population générale pour les pathologies autosomiques récessives. Dans ce contexte, le rendement diagnostique constaté est faible, comme c’est le cas dans des pathologies comme l’amyotrophie spinale avec 478 examens demandés et un seul fœtus atteint sur la période 2019-2023 ; et dans une moindre mesure pour la mucoviscidose avec 76 fœtus atteints pour 1 126 examens. Un autre exemple est celui du syndrome de Prader-Willi, avec 906 examens réalisés sur signe d’appel échographique, sans antécédent familial, sur la période 2019-2023, et 26 fœtus atteints.
L’utilisation d’étude par panels de gènes s’est stabilisée par rapport à l’année dernière avec un nombre d’examens comparable (140) pour un même nombre de laboratoires (9).
En revanche, 19 laboratoires indiquent avoir réalisé des techniques d’analyse de l’exome, versus 13 en 2022. On note, comme depuis 2019, une progression continue, importante du nombre d’examens de séquençage d’exome prénatal qui a plus que doublé entre 2022 et 2023 (1 298 versus 614 examens). Ces derniers ont porté un diagnostic moléculaire d’atteinte fœtale dans 25% des cas (318 sur 1298) (tableau DPN20).
L’ensemble de ces données sont en faveur d’un recours de plus en plus conséquent aux techniques de NGS en DPN, avec utilisation majoritaire du séquençage d’exome.
Lorsqu’un diagnostic de maladie génétique d’une particulière gravité non curable au moment du diagnostic est confirmé, une demande d’IMG peut être demandée par la femme au CPDPN. Les informations relatives aux issues de grossesses sont publiées dans le cadre du rapport d’activité des CPDPN.

On entend par prélèvement non invasif un prélèvement sanguin chez la femme enceinte, par opposition aux prélèvements dits invasifs (comme par exemple d’un prélèvement de tissus annexiel ou embryonnaire). Ces analyses se sont considérablement développées ces dernières années et méritent d’être particulièrement suivies.
Actuellement, les indications pour une analyse de l’ADN fœtal libre circulant dans le sang maternel (ADNlc) ayant fait l’objet d’une recommandation de la Haute Autorité de Santé (HAS) sont :
• L’analyse du rhésus fœtal chez les femmes rhésus négatif,
• La détermination du sexe fœtal pour les indications de « fœtus à risque pour une maladie génétique liée à l'X » et de « fœtus à risque pour l'hyperplasie congénitale des surrénales ».
Nous présentons également dans ce rapport les données relatives au diagnostic prénatal non invasif de maladies monogéniques.
Dans son rapport de 2011, la HAS précise que la détermination prénatale du génotype fœtal RhD à partir du sang maternel présente un intérêt en pratique clinique pour cibler les populations devant bénéficier d’injection prophylactique d’immunoglobulines anti-RH1, ainsi qu’en cas d’immunisation, pour sélectionner les femmes devant bénéficier d’un suivi spécialisé. Cet examen bénéficie d’une prise en charge par l’assurance maladie depuis juin 2017. Depuis 2019 le nombre de déterminations est relativement stable. En 2023, 71 361 déterminations ont été réalisées, soit une diminution de 5% des examens par rapport à 2022, dans un contexte de diminution du nombre de naissances vivantes de l’ordre de 6,6% sur la même période (Tableau DPN21). La proportion des grossesses étudiées avec un fœtus Rh- en 2022 est comparable à celle entre 2019 et 2023, hormis une baisse importante observée en 2021. Le rhésus fœtal est RhD- pour 23 566 soit 33% grossesses dépistées en 2023 (Tableau DPN22). La proportion, qui reste faible, de typage fœtal autre que rhésus est de 1%, avec 745 fœtus sur 71361 soit versus 0,9% en 2022, et a doublé depuis 2019 (0,5%).
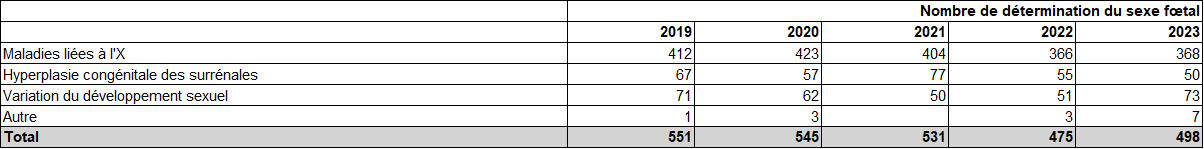
La détermination du sexe fœtal dans le sang maternel n’est autorisée que dans des indications très spécifiques et représente 498 examens en 2023. L’indication majoritaire avec 74 % des déterminations, est représentée par les maladies liées au chromosome X, majoritairement pour pouvoir proposer en cas de fœtus de sexe masculin pour une pathologie récessive liée à l’X, un prélèvement fœtal invasif précoce durant la grossesse et pouvoir l’éviter en cas de sexe féminin fœtal. Pour les grossesses à risque d’hyperplasie congénitale des surrénales, qui représentent 50 examens, soit 10% de l’ensemble, proportion la plus basse depuis 2019, la détermination du sexe fœtal a pour but de prévenir le risque de virilisation chez un fœtus féminin, en permettant la mise en route d’un traitement dédié précoce en cas de fœtus de sexe féminin. En 2023, une variation du développement sexuel représente la dernière indication déclarée avec 73 examens, soit 14,7% des indications (tableau DPN23). Concernant l’indication « autres », 7 déterminations ont été déclarées par un seul laboratoire dont nous allons nous rapprocher afin de préciser sa pratique.
Les examens pour convenance personnelle sont interdits en France.
Le diagnostic non invasif par l’examen de l’ADN libre circulant dans le sang maternel représente une véritable alternative au diagnostic prénatal invasif de récurrence de certaines maladies monogéniques. A l’heure actuelle, les situations de recours à ces examens sont basées sur la possibilité de diagnostics d’exclusion. Le principe de cet examen est la recherche de variant pathogène d’origine paternelle dans le cas de maladies transmises selon un mode autosomique récessif ou dominant, ou la recherche d’une variation pathogène survenue de novo dans l’ADN fœtal.
Le tableau DPN24 montre une augmentation du recours à ces examens ces 5 dernières années.
En 2023, 331 examens ont été réalisés. La recherche de variant pathogène se fait le plus fréquemment au sein du gène FGFR3 dans le cas de suspicion d’achondroplasie (61 examens) et de dysplasie thanatophore (13 examens), l’exclusion de la mutation paternelle dans le gène CFTR, responsable de la mucoviscidose (50 examens), et dans le gène NF1 responsable de neurofibromatose de type 1 (6 examens). Pour le diagnostic d’exclusion de la mutation paternelle dans d’autres gènes, soit 201 examens, celui-ci n’a concerné qu’un à deux DPN chacun.
L’harmonisation des pratiques est en cours au niveau des professionnels, et sera rediscutée au sein du groupe de travail dédié au DPN.